| Investigador Principal (IP): Gago Domínguez, Manuela | Código: PI12/02125 | ||
| Convocatoria: ayudas Acción Estratégica en Salud 2012 (AES 2012) – ISCIII | |||
| Presupuesto: 139.295,90€ | Fecha inicio:dd/mm/2012 | Duración: 3 años | |
| Objetivos:
Al plantear este estudio, se perseguían los siguientes objetivos: 1. La realización de un estudio caso-control evaluando el papel de productos de la peroxidación lipídica (PL)o isoprostanos(isoP) en orina y muestras de aspirado de pezón (NAF, siglas en inglés), en el desarrollo del cáncer de mama (CM). 1.1. Determinar si el efecto de los factores de protección ya establecidos para el CM, incluyendo edad temprana a primer embarazo/ a término, elevada paridad, ooforectomía, edad tardía de menarquia, edad temprana de menopausia, obesidad pre-menopáusica y actividad física, está asociado con niveles elevados de isoP en orina y/o NAF. 1.2. Determinar si el incremento en el riesgo para CM de factores de riesgo establecidos, incluyendo estatura, ingesta de alcohol, terapia de reemplazo hormonal, y obesidad postmenopaúsica, está asociado con niveles disminuidos de isoP en orina y/o NAF. 2. Determinar si el aumento en el riesgo de CM de los loci de susceptibilidad identificados a través de estudios GWAS, está asociado con el nivel de los isoP en orina y/o NAF Palabras clave:cáncer de mama (CM), tumor maligno, peroxidación lipídica (PL), isoprostanos (isoP), niveles sangre/ orina, aspirado de pezón (NAF en inglés),herramienta de diagnóstico, factores de riesgo/ protección, loci, variaciones genéticas,MassARRAY, Genome-Wide-Association-Screening (GWAS), Single-Nucleotide Polymorphims (SNPs), análisis estadístico. |
|||
EQUIPO
| Apellidos | Nombre | Titulación/ Categoría y Entidad |
| Gago Domínguez | Manuela | Medicina, doctor/ IP(*) CHUS |
| Carracedo | Angel | Medicina, doctor/ Colaborador, FPGMX |
| Castelao | Esteban | Medicina, doctor/ Investigador, CHUVI |
| Novo Domínguez | Alejandro | Medicina, doctor/Jefe de Servicio- Ginecología, CHUS |
| Peña | Maite | Medicina, doctora/ Adjunta – Ginecología, CHUS |
| Redondo | Carmen | Química Computacional, doctora/ Investigadora, CHUVI |
| Ruíz Larrea | Mª Begoña | Medicina, doctora/ Profesora universitaria, UPV |
| Ruíz Sanz | José Ignacio | Medicina, doctor/ Profesor universitario, UPV |
| Torres | María | Biología Molecular, licenciada/ Colaboradora, CEGEN |
| ND | ND | Personal enfermería/ colaboradores,(CHUS, CHUVI), |
| ND | ND | Técnico de laboratorio/ colaboradores(CHUS, FPGMX, UPV) |
IP: Investigador Principal
ENTIDADES PARTICIPANTES Y COLABORADORAS
| Nombre | Siglas | Tipo/ Categoría |
| Centro Nacional de Genotipado,
Nodo en Galicia del Instituto de Salud Carlos III |
CEGEN /
ISCIII |
Organismo público /
Asistencial e investigación clínica |
| Fundación Pública Galega de Medicina Xenómica | FPGMX | Organismo público |
| Complexo Hospitalario Universitario de Santiago | CHUS | Hospital público |
| Complexo Hospitalario Universitario de Vigo | CHUVI | Hospital público |
| Servizo Galego de Saúde | SERGAS | Organismo público |
| Universidad del País Vasco | UPV | Organismo público |
| Universidade de Santiago de Compostela | USC | Organismo público |
Antecedentes e hipótesis de partida
El cáncer de mama (CM) es actualmente el tumor maligno más frecuente entre las mujeres, por lo que es esencial desarrollar una herramienta de evaluación del riesgo de CM. La existencia de dicho (bio-)marcador/ herramienta, debierafacilitar la identificación de mujeres con riesgo elevado y lograr incrementar las posibilidades de supervivencia de las pacientes, al permitir una intervención más temprana.A día de hoylas dos pruebaspara la detección de CM recomendadas por la Sociedad Americana del Cáncer son el examen clínico de los senos y la mamografía.Mediante éstaúltima, sin embargo, no se detectan entre un 20-30% de los cánceres (hablamos de 350 mujeres por cada 100.000 con CM y con edades comprendidas entre75-105), ya que el CM puede yacer oculto por otro tejido denso de la mama. Así mismola mamografía no detecta cambios anormales hasta 8 años después de que éstos se inicien y a las mujeres menores de 40 años, no se les realizan mamografías.
La evidencia experimental, en la fecha de inicio de este estudio, sugería que la más poderosa y consistente influencia en la protección del CM estaba directamente relacionada con la generación de productos de la PL. Múltiples estudios sugerían que un aumento en los niveles de dichos productosdesempeñaba un importante papel protector. Así la inhibición del crecimiento del CM por los ácidos grasos poli-insaturados, tales como los omega 3 (AG n-3), alpha-linolénico, conjugado linoleico y gamma linolénico (GLA), tanto in vivo como in vitro,está directamente relacionada con la generación de PL en las células tumorales. Por ello la presencia de compuestos resultantes de la PL, los isoP, en muestras de orina y aspirado de pezón, eran una opción prometedora como (bio-)marcadores/ herramientas.
La PL desempeña pues un papel induciendo la apoptosis y constituye por ello un mecanismo protector en la carcinogénesis de mama (1-4). Los isoP, medidos en orina o en NAF, podrían ser marcadores efectivos para el cribado de CM (1-4) y un estudio de un tamaño muestraladecuado,determinaría si las mujeres diagnosticadas con CM exhiben niveles disminuidos de isoP, en comparación con aquellas no diagnosticadas.
Así mismo,se estudiará el papel y/o factor genético en el CM, es decir, aquellas variantes genéticas comunes que se asocian con el riesgo de padecerlo/ desarrollarloy que hayan sido identificados gracias a estudios deGenome-Wide-Association-Screening(GWAS).Los GWAS han surgido como un enfoque nuevo y poderoso para identificar loci de susceptibilidad de baja penetrancia.
Referencias:
(1) Gago-Domínguez M, Castelao J, Pike MC et al.Cancer Epidem Biom Prev 2005;14:2829-39.
(2) Gago-Dominguez M, Jiang X, Castelao JE. Breast Cancer Res 2007;9:201.
(3) Gago-Dominguez M, Jiang X, Castelao JE. Med Hypotheses 2007;68:1138-43.
(4) Gago-Dominguez M, Castelao JE. Crit Rev in Oncology/Hematology 2008;68:107-14.
Población de estudio.
Las mujeres participantes en el estudio (casos y controles) fueron identificadas en el Servicio de Ginecología del Complexo Hospitalario Universitario de Santiago (CHUS). Se trataba de mujeres de entre 20 y 85 años de edad, no embarazadas, con CM incidente (confirmado clínica o histológicamente), sin tratar, que no hubieran sido diagnosticadas con otro tipo de cáncer en los últimos 5 años (excepto cáncer de piel de tipo no melanocítico) y que dieron su consentimiento por escrito. Los controles eran mujeres de entre 20 y 85 años de edad, no embarazadas, sin historia previa de cáncer (excepto cáncer de piel de tipo no melanocítico) que dieron su consentimiento por escrito. Casos y controles fueron apareados en función de la edad (± 5 años).
En cuanto al tamaño del muestreo, se estimó en función del origen de las muestras:
– orina: se tomaron500 muestras de cada (casos y controles) para tener un 90% de potencia que permitiese detectar una asociación (OR=0.7-0.8) entre los niveles de los isoP y el riesgo de CM, usando un modelo de regresión logística (programa nQueryAdvisor 7.0 (1) con un nivel de significancia del0.05yuntestbilateral).
– NAF: de entre las 500 mujeres iniciales con CM, la colección de muestra se realizó en 150 mujeres que cumplían el requisito de ser premenopáusicas. Así con 150 casos y 150 controles,se obtendría también unapotencia del 90%, detectándose una asociación (OR=0.6-0.7) entre los niveles de los isoP y el riesgo de CM, usando el mismo modelo de regresión logística que para las muestras de orina.
http:// statistical-solutions-software.com
Publicaciones y estado del arte previos a la realización de este estudio
Gago-Domínguez M, Castelao J, Pike MC et al. Cancer Epidemiol Biomarkers Prev 2005;14:2829-39.
Gago-Domínguez M, Jiang X, Castelao JE. Breast Cancer Res 2007;9:201.
Sun SY, Hail N, Jr., Lotan R. J Natl Cancer Inst 2004;96:662-72.
Gago-Dominguez M, Jiang X, Castelao JE. Med Hypotheses 2007;68:1138-43.
Gago-Domínguez M, Castelao JE. Critical Reviews in Oncology/Hematology 2008;68:107-14.
Gago-Domínguez M, Castelao JE. Free Radical Biology & Medicine 2006;40:721-33.
Schor NF, Tyurina YY, Tyurin VA, Kagan VE. Biochem and Biophys Res Communications 1999;260:410-5.
Teixeira C, Reed JC, Pratt MA. Cancer Research 1995;55:3902-7.
Chajes V, Mahon M, Kostner GM. Free Radical Biology & Medicine 1996;20:113-20.
Early Breast Cancer Trialists’ Collaborative Group. Lancet 1998;351:1451-67.
Menendez JA, Vellon L, Colomer R, Lupu R. J. Natl. Cancer Inst. 2005;97:1611-5.
Das UN. Prostaglandins Leukotrienes and Essential Fatty Acids 1999;61:157-63.
Mannello F, Tonti GA, Pagliarani S, et al. Int J Cancer 2007;120:1971-6.
Chen G, Djuric Z. Cancer Epidemiol Biomarkers Prev 2002;11:1592-6.
Petrakis NL, Gruenke LD, Craig JC. Cancer Res 1981;41:2563-5.
Dai Q, Gao YT, Shu XO et al. Official journal of the American Society of Clinical Oncology 2009;27:2482-8.
Milne GL, Yin H, Brooks JD, et al. Methods Enzymol 2007;433:113-26.
Nourooz-Zadeh J. BiochemSoc Trans 2008;36:1060-5.
Kadiiska MB, Gladen BC, Baird DD, et al. Free RadicBiol Med 2005;38:698 – 710.
Gago-Domínguez M, Yuan JM, Sun CL, et al. British Journal of Cancer 2003;89:1686-92.
Gago-Dominguez M, Castelao JE, Sun CL, et al. Carcinogenesis 2004;25:2143-7.
Brooks M. Methods MolBiol 2009;472:307-21.
Easton DF, Pooley KA, Dunning AM, et al. Nature 2007;447:1087-93.
Gold B, Kirchhoff T, Stefanov S, et al. Proc Nat Acad of Sci USA 2008;105:4130-5.
Stacey SN, Manolescu A, Sulem P, et al. Nature Genetics 2007;39:865-9.
Hunter DJ, Kraft P, Jacobs KB, et al. Nature Genetics 2007;39:870-4.
Stacey SN, Manolescu A, Sulem P, et al. Nature Genetics 2008;40:703-6.
Thomas G, Jacobs KB, Kraft P, et al. Nat Genet 2009;29:29.
Ahmed S, Thomas G, Ghoussaini M, et al. Nat Genet 2009;41:585-90.
Zheng W, Long J, Gao YT, et al. Nat Genet 2009;41:324-8.
Liang J, Chen P, Hu Z, et al. Carcinogenesis 2008;29:2131-6.
McInerney N, Colleran G, Rowan A, et al. Breast Cancer Res and Treatment 2009;117:151-9.
Raskin L, Pinchev M, Arad C, et al. Cancer epidem, bioma&prev 2008;17:1060-5.
Rebbeck TR, DeMichele A, Tran TV, et al. Carcinogenesis 2009;30:269-74.
Bao S, Wang Y, Sweeney P, et al. Am J Physiol Lung Cell MolPhysiol 2005;288:L36-42.
Pan ZZ, Devaux Y, Ray P. MolBiol Cell 2004;15:3106-13.
Crescioli C, Maggi M, Luconi M, et al. Prostate 2002;50:15-26.
Hines MD, Allen-Hoffmann BL. J BiolChem 1996;271:6245-51.
Wildhaber BE, Yang H, Teitelbaum DH. J PediatrSurg 2003;38:92-6; discussion -6.
Zheng WJ, Yuan L, Liu XD, Zheng D. J Forestry Res 2005;16:335-8.
Braun S, Krampert M, Bodo E, et al. J Cell Sci 2006;119:4841-9.
Ray P, Devaux Y, Stolz DB, et al. Proc Natl AcadSci U S A 2003;100:6098-103.
Barazzone C, Donati YR, Rochat AF, et al. Am J Pathol 1999;154:1479-87.
Wu KI, Pollack N, Panos RJ, et al. Am J Physiol 1998;275:L780-7.
Cox A, Dunning AM, Garcia-Closas M, et al. Nature Genetics 2007;39:352-8.
Grenet J, Teitz T, Wei T, et al. Gene 1999;226:225-32.
Jongstra-Bilen J, Jongstra J. Immunol Res 2006;35:65-74.
Howard T, Li Y, Torres M, et al. Blood 1994;83:231-41
En la tabla 1 se indican características y resultados de GWAS publicados hasta la fecha para CM:
| Estudio y resultados de GWAS publicados para Cáncer de Mama | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Referencia
estudio |
Diseño | Población | Plataforma
genotipado [SNPs] |
SNPs
[frecuencia alelo] |
Región/gen | OR | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Easton 200723
Ahmed 200929 |
Estudio BCAC
4-etapas, caso-control |
1ª etapa: 390 casos, 364 controles;
2ª etapa: 3.990 casos, 3.916 controles 3ª etapa: 21.860 casos, 988 CIS,and 22.578 controles 4ª etapa: 33.134 casos, 36.141 controles |
High density oligonucleotide,
Sphotolithographic at Perlegen Sci. |
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hunter 200726
Thomas 200928 |
3-etapas: 9.770 casos y 10.799 controlesIniciativa CGEMS. | 1ª etapa: 1.145 casos, 1.142 controles
2ª etapa: 4.547 casos, 4.434 controles. 3ª etapa: 4.078 casos, 5.223 controles |
Illumina HumanHap500 |
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stacey 200725
Stacey 200827 |
2-etapas,
caso-control |
1ª etapa: 1,600 casos, 11,563 controles.
2ª etapa: 6,145 casos, 33,016 controles |
Illumina HumanHap300 |
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gold 200824
|
3-etapas caso-controlentre judíos Ashkenazi | 1ª etapa: 249 casos, 299 controles.
2ª etapa: 950 casos, 979 controles. 3ª etapa: 243 casos, 187 controles |
Affymetrix EAv3
500k |
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Zheng 200930 | 3-etapas caso-controlen población china | 1ª etapa: 1,505 casos, 1,522 controles.
2ª etapa: 1,554 casos, 1,576 controles. 3ª etapa: 3,472 casos, 900 controles |
Affymetrix 500k
Human SNP array 6.0 |
rs2046210 [0.36] | 6q25.1,ESR1 |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| * Frecuencia menor de un alelo en el estudio SEARCH estudio. # MAF entre controles NHS; $ OR heterozigoto | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Tabla 1
Población de estudio. Análisis estadístico y genético
Las mujeres participantes en el estudio (casos y controles) fueron identificadas en el Servicio de Ginecología del Complexo Hospitalario Universitario de Santiago (CHUS). Se trataba de mujeres de entre 20 y 85 años de edad, no embarazadas, con CM incidente (confirmado clínica o histológicamente), sin tratar, que no hubieran sido diagnosticadas con otro tipo de cáncer en los últimos 5 años (excepto cáncer de piel de tipo no melanocítico) y que dieron su consentimiento por escrito. Los controles eran mujeres de entre 20 y 85 años de edad, no embarazadas, sin historia previa de cáncer (excepto cáncer de piel de tipo no melanocítico) que dieron su consentimiento por escrito. Casos y controles fueron apareados en función de la edad (± 5 años).
En cuanto al tamaño muestral, según el origen de las muestras:
– orina: se tomaron500 muestras de cada (casos y controles) para tener un 90% de potencia que permitiese detectar una asociación (OR=0.7-0.8) entre los niveles de los isoP y el riesgo de CM, usando un modelo de regresión logística (programa nQueryAdvisor 7.0 (1) con un nivel de significancia del0.05yuntestbilateral).
– NAF: de entre las 500 mujeres iniciales con CM, la colección de muestra se realizó en150 mujeres que cumplían el requisito de ser premenopáusicas, porque sehabíaobservado que la produccióndeNAFeramuyreducidaeneste colectivo(2,3,4). Así con 150 casos y 150 controles,se obtendría también unapotencia del 90%, detectándose una asociación (OR=0.6-0.7) entre los niveles de los isoP y el riesgo de CM, usando el mismo modelo de regresión logística que para las muestras de orina.
En cuanto a las variables, para cada paciente y/o participante en el estudio se recogieron, vía cuestionario de factores de riesgo para CM, los datos que se indican en la tabla siguiente:
| Nr. | Variables | Nr. | Marcadores |
| 1 | Edad(es) | 11 | IsoProstanos |
| al diagnóstico | iPF2α-III, iPF2α-VI, 8,12- iPF2α-VI,
2,3-dinor-iPF2α-III, d4-5-epi-8,12-iPF3α-VI; d4,12-8-iPF3α-VI |
||
| a la menarquía | |||
| a la menopausia
(si procede) |
|||
| 2 | Menopausia | 12 | (n= 27) SNPs a analizar en cromosomas: |
| Tipo de menopausia
(natural, quirúrgica) |
10q26 [FGFR2: rs2981582, rs10510126, rs1219648,
rs2420946, rs1078806] |
||
| Si menopausica, uso de terapia
hormonal de reemplazo(?) |
16q12 [TOX3: rs1244362, rs8051542, rs3803662] | ||
| 3 | Uso anticonceptivos hormonales | 11p15 [LSP1:rs3817198; H19:rs2107425] | |
| 4 | Embarazo | 5p12 [MRPS30:rs4415084, rs10941679, rs981782] | |
| Número | 5q11 [rs30099; MAP3K1:rs889312] | ||
| Edad al término del 1º | 8q24 (rs1281615) | ||
| Problemas de salud (?) | 6q22 [ECHDC1: rs2180341] | ||
| 5 | Lactancia materna | 2q35 (rs13387042) | |
| 6 | Enfermedades | 2p (rs4666451) | |
| antecedentes familiares cáncer
(CM en este caso particular) |
7q22 [RELN:rs17157903] | ||
| Diagnósticadas | 4p14 [TLR1/TLR6:rs7696175; rs12505080] | ||
| 7 | Medicamentos de uso crónico | 1p11 [NOTCH2/FCGR1B: rs11249433] | |
| 8 | Hábitos de consumo | 14q24 [RAD51L1:rs999737] | |
| Alcohol | 3p24 [SLC4A7/NEK10: rs4973768] | ||
| Tabaco | 17q23 [COX11: rs6504950] | ||
| 9 | Datos talla | 6q25 [ESR1:rs2046210] | |
| Peso (actual) | |||
| Antes/ después menopausia | |||
| Altura | |||
| 10 | Nivel de actividad física |
Tabla 2
En cuanto al análisis estadístico:
– niveles deisoPyriesgo de CM:seusaron (i) histogramas por separado, para casos y controles,(ii) modelosderegresiónlogística paraanalizar laasociación entreelriesgodepadecer CMyelniveldelosisoP(engeneral oestratificados, según el nivel de los otros marcadores)y (iii)curvasROCexperimentales,paraevaluarlaexactituddelosdistintosisoPalahoradepredecirelriesgo de CM.
Se tuvieron en cuenta así mismo el sexo y la edad en los análisis univariantesy, en el caso de los multivariantes, factoresambientalesygenéticosderiesgoparaelCM. Ante la posibilidad de que el propio crecimiento del tumor pudiera modificar el marcador seleccionado, estudiamos el marcadorestratificadoporestadioygradodediferenciacióntumoral.Hay que destacar que, en la fecha de planificación, sólo exstía un estudio/ precedente en el que se hubieran examinadolos nivelesdeisoPenNAFenrelación conelestadíodeltumor (5,6).
En cuanto al análisis genético :
– comprobación de la asociación entre las variaciones genéticas (esto es, 27 SNPs) y niveles de los distintos marcadores: se usaron un modelo de regresión lineal del tipo Yi=a + b1’Zi+b2’Giy el test de Armitage [basado en un modelo log- aditivo para la herencia (7)]. Para todo ello se recurrió al PLINK(8).
Referencias:
http:// statistical-solutions-software.com
Bentz J. Oncology News 2009; 4(1): 8-9
Petrakis NL. Cancer Epidemiol biomarkers Prev 1993; 2(1): 3-10.
Jiang X, Castelao JE, Chavez-Uribe E et al. PLoS One 2012; 7(1):e29459. Epub 2012 Jan 6
Kato I, Ren J, Heilbrun LK, Djuric Z. Biomarkers 2006; 11:143-52.
Mannello F, Tonti GA, Pagliarani S, et al. Int J Cancer 2007; 120: 1971-6.
Yen Y, Kraft P. Genetic Epidemiology 2005; 29: 289.
Purcell S, Neale B, Todd-Brown K, et al. Am J HumGenet 2007; 81:559-75.
Metodología. Cronograma y Trabajo realizado
Reclutamiento pacientes y recogida de muestras.Las candidatas a participar en este estudio fueron informadas por su ginecólogo habitual y, aquellas que accedieron a participar, donaron muestras de sangre, orina y líquido de aspirado de pezón. Las muestras de orina y NAF se enviaron posteriormente a la UPV y las de sangre a la FPGMX, procediéndose a su análisis.
Cuestionarios.Recurrimos a cuestionarios de factores de riesgo para CM, validados por el Instituto Nacional de Salud de los EEUU (NCI), y que habían sido ya empleados satisfactoriamente en los estudios ELLA del MD Anderson y la Universidad de Arizona (1)
Análisis de muestras.
Marcadores de peroxidación lipídica en muestras de NAF y orina: dichas muestras fueron analizadas por los doctores Ruíz Larrea y Ruíz Sanz en sus laboratorios de la UPV, según lo planeado, y mediante las técnicas de GC/MS descritas en bibliografía para tal fin (2,3).
De genes:el genotipado de las muestras de ADN genómico (muestras de sangre), se realizó en el CeGen-ISCIII del la USC mediante el método SequenomMassARRAY(estrategia de SBE,single base extensión). La detección de los productos se hizo por espectrometría de masas MALDI-TOF, empleándose2 μL de ADN/ reacción, a una concentración de 10 ng/μL, y llegándose a analizar hasta 36 SNPs/reacción (4).
Análisis de datos. Los datos extraídos de los cuestionarios de factores de riesgo para CM, la historia clínica y los resultados de los análisis de las muestras, se procesaron mediante los métodos y el software estadístico disponible, esto es, R, SPSS y PLINK.
Referencias:
(1) www.ellastudy.medicine.arizona.edu/
(2) Lawson JA, Rokach J, Fitzgerald GA. J BiolChem 1999; 274:24441-4.
(3) Schwedhelm E, Boger RH. Clin Chem Lab Med 2003; 41: 1552-51.
(4) Buetow KH, Edmonson M, MacDonald R, et al. PNAS 98 (2001): 581-4.
Limitaciones. No/ Si se observaron las previsibles, esto es, en cuanto a la potencia para detectar errores genéticos menores (R2<0.06). Tampoco se reportaron incidencias destacables, relativas a la toma de muestras (NAF, orina y/o sangre).
Aspectos ético- legales. El estudio se llevó a cabo tal y como se planteó en la propuesta inicial, según la declaración de Helsinki de la Asamblea Médica Mundial de 1996 y de las normas de Buena Práctica Clínica de la Conferencia Internacional de Armonización. Así mismo el estudio fue aprobado por el Comité Ético de Investigación Clínica de Galicia y todas las participantes en el mismo dieron consentimiento informado por escrito.
Cronograma. El estudio se realizó/ está realizando en el tiempo estimado según el cronograma a continuación:
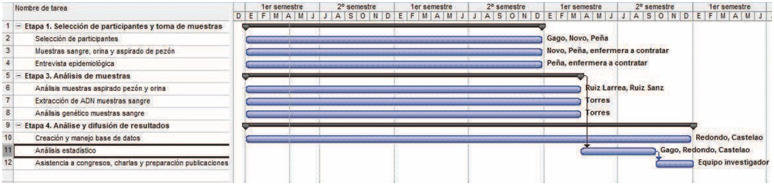
| Tareas/ actividades | Etapas e Hitos | Recursos | Lugar | |
| 1 | Selección de participantes y toma de muestras | |||
| 1a | Selección de participantes, invitación a participar en el estudio | Historias clínicas individuales | Servicio Ginecología,
CHUS |
|
| 1b | Toma de muestras de sangre, orina y aspirado de pezón | Bombas sacaleche.
Tubos y frascos para recogida muestras, de sangre y muestras de orina. |
||
| 1c | entrevista epidemiológica de factores de riesgo para el CM | Cuestionarios | ||
| 2 | Análisis de muestras | |||
| 2a | Análisis de muestras de orina y aspirado de pezón para determinar losniveles de marcadores de peroxidación lipídica | Análisis (a subcontratar) | UPV | |
| 2b | Extracción ADN muestras de sangre | Medios y material para extracción de ADN | CeGen_ISCIII,
USC |
|
| 2c | análisis genético de las muestras de ADN | Análisis | CeGen_ISCIII,
USC |
|
| 3 | Análisis de datos | |||
| 3a | Creación y manejo base de datos.
Introducción de datos recogidos |
Ordenadores y
programas informáticos |
CHUVI | |
| 3b | Análisis estadístico de los datos obtenidos | CHUVI | ||
| 3c | Asistencia a congresos, charla.
Preparación de publicaciones |
Todo el EQUIPO |
Aspectos ético- legales. El estudio se llevó a cabo tal y como se planteó en la propuesta inicial, según la declaración de Helsinki de la Asamblea Médica Mundial de 1996 y de las normas de Buena Práctica Clínica de la Conferencia Internacional de Armonización. Así mismo el estudio fue aprobado por el Comité Ético de Investigación Clínica de Galicia y todas las participantes en el mismo dieronconsentimiento informado por escrito.
Resultados y publicaciones asociados
ND





